Hirnmetastasen
Unsere modernen Behandlungsmethoden von Metastasen und Tumoren im Kopf oder Körper sind gut erprobt und weltweit anerkannt. Die Behandlung ist bei Metastasen eine schmerzlose, ambulante und sichere Therapie. Speziell das ERCM hat sehr große Erfahrung auf diesem Gebiet und bietet Patienten mit Hirnmetastasen eine gut erprobte und sichere Behandlungsmethode an.
Bei einer Metastasen-Behandlung entfällt das Risiko für Komplikationen, die bei einer klassischen Operation auftreten können. Die Therapie ist für Patienten komfortabel, weil sie ohne eine Fixierung, ohne Narkose und ohne offene Operation behandelt. Ein stationärer Krankenhausaufenthalt ist daher nicht erforderlich. Patienten können den gewohnten Aktivitäten in den meisten Fällen im Anschluss an die Behandlung nachgehen.
Form, Gestalt und Struktur
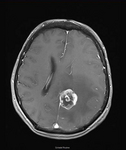
Über zwei Drittel der innerhalb des Schädels liegenden Metastasen liegen oberhalb des Kleinhirns (supratentoriell). Primärtumore aus dem kleinen Becken und den Gastrointestinalentrakt neigen bevorzugt zu einer infratentoriellen (unterhalb des Kleinhirns liegend) Metastasierung. Die Gründe für dieses Phänomen sind unklar. Hirnmetastasen sind rundlich- oder ovalkonfigurierte Läsionen, verdrängen das gesunde Gewebe und wachsen in der Regel nicht infiltrierend (nicht ins Gewebe eindringend). Sie liegen vorzugsweise im Grenzbereich zwischen der weißen und grauen Substanz und im Bereich der vaskulären Grenzlinien (Russel and Rubinstein, 1989; Hwang et al. 1996).
Häufigkeit
Hirnmetastasen stellen mehr als die Hälfte der intracraniellen Tumoren dar. Sie werden bei 10 bis 30 % der Erwachsenen und 6 bis 10 % der Kinder mit malignen Tumoren diagnostiziert. In den USA werden jährlich zwischen 98.000 und 170.000 neue Fälle registriert (Johnson et al. 1996). Bei ca. 20 % der Patienten stellen die Hirnläsionen die einzige metastatische Tumormanifestation dar, während bei 80 Prozent auch extrazerebrale Metastasen diagnostiziert wurden.
Bronchialkarzinome, maligne Melanome, Mammakarzinome, Hypernephrome und Colorektalkarzinome sind die häufigsten Tumorentitäten, die zu einer Hirnmetastasierung führen. Kopf-Hals-Tumoren, andrologische und gynäkologische Tumoren sowie Knochen- und Weichteilsarkome metastasieren selten intrakraniell (Mehta et al. 1992).
Diagnostik
Hirnmetastasen sind durch eine pathologische Blut-Hirnschranke charakterisiert und stellen sich in der Bildgebung (CT und MRT) als stark kontrastmittelaufnehmende Strukturen mit perifokalem Ödem dar. Die MRT zeigt eine höhere Sensitivität als die CT, insbesondere die T1 gewichteten Aufnahmen nach erhöhter Gadoliniumapplikation. Als Differenzialdiagnosen können hirneigene Tumoren, entzündliche Erkrankungen oder Meningeome diskutiert werden. Funktionelle Untersuchungen wie PET, SPECT und MR-Spektroskopie können für die Differenzialdiagnose Tumor versus Nekrose nach einer Strahlentherapie nützlich sein. Eine komplette aktuelle Staging-Untersuchung ist für die Entscheidung für eine oder andere therapeutische Strategie sehr wichtig.
Die Biopsie ist indiziert bei Patienten mit unklarem radiologischem Befund, mit unbekanntem Primärtumor oder mit unklarer onkologischer Anamnese, z.B. bei großem Zeitabstand zwischen der Diagnose des Primärtumors und der Hirnmetastasierung.
Therapie
Mikrochirurgie, Radiochirurgie (z.B. Cyberknife-Therapie), Ganzhirnbestrahlung (GSB), stereotaktische fraktionierte Strahlentherapie (SFS), Chemotherapie und alleinige symptomatische Behandlung sind die wichtigsten therapeutischen Optionen. Die letztendliche Entscheidung ist abhängig vom klinisch-neurologischen Status des Patienten, von der Aktivität des Primärtumors und der Anzahl und Lokalisation der Metastasen.
Symptomatische Therapie
Die alleinige symptomatische Therapie mit Cortisonpräparaten reduziert das perifokale Ödem und mildert vorübergehend die neurologischen Beschwerden. Die Präparate mit Dexamethason haben, im Vergleich zu den anderen Corticosteroiden, den Vorteil eines niedrigeren Risikos von Nebenwirkungen (Ödemen, Hypokaliämie, Infektionen, Psychose etc.). Die Dosierung hängt von der klinischen Symptomatik und Ausdehnung des Ödems ab. Bei Patienten mit epileptischen Anfällen ist eine Antiepileptikatherapie sinnvoll.
Radiochirurgie (Cyberknife–Therapie)
Hirnmetastasen mit einem maximalen Durchmesser kleiner als 3 cm stellen ein ideales Target für die Cyberknife-Therapie dar. Die lokale Tumorkontrolle liegt bei ca. 90 %. Wissenschaftliche Analysen haben bewiesen, dass in der Behandlung selektionierter Patienten mit Hirnmetastasen die Radiochirurgie der Operation mindestens gleichwertig ist bei erheblich größerem Patientenkomfort (Muacevic 2005).
Generell wurde beobachtet, dass die Histologie des Primärtumors für die Tumorkontrolle und das Ansprechen nach Radiochirurgie keine statistische Signifikanz hat (Grosu et al. 2000). Sogenannte strahlenresistente Entitäten wie zum Beispiel maligne Melanome und Hypernephrome zeigen eine sehr gute lokale Tumorkontrolle nach Einzeitbestrahlung (Engenhart et al. 1993; Alexander et al. 1995). Die wichtigste Nebenwirkung der Therapie ist die Strahlenreaktion, die mit einer Häufigkeit von ca. 2 bis 5 % auftritt und meist mit Cortison behandelt wird.
Mikrochirurgie
Eine klare Indikation zur operativen Therapie besteht bei oberflächlich gelegenen, größeren Metastasen oder bei Tumoren, die durch Massenverschiebung eine progrediente neurologische Symptomatik verursachen. Bei Herden in der hinteren Schädelgrube kann durch die Größe der Metastase, oder auf Grund eines ausgeprägten perifokalen Ödems die Gefahr einer zerebralen Herniation oder eines Hydrocephalus occlusus bestehen. Hier ist eine notfallmäßige operative Entfernung der Metastase angezeigt (Reulen et al. 1995).
Unabhängig von der Art der Therapie ist für die Gesamtprognose, neben der Kontrolle des Primärtumors, der klinische Zustand des Patienten vor der Behandlung entscheidend. Patienten in gutem klinischem Zustand überleben bei Anwendung beider möglicher Verfahren (Operation oder Strahlentherapie) signifikant länger als Patienten in schlechterem klinischen Zustand (Karnofsky Performance Score < 70). Andere prognostische Faktoren wie Alter des Patienten, Tumorlokalisation, Art des Primärtumors und auch die Latenzzeit zwischen Diagnosestellung des Primärtumores und Auftreten der zerebralen Metastase spielen eine untergeordnete Rolle (Muacevic et al. 1999).
Metastasen des kleinzelligen Bronchialkarzinoms, maligner Lymphome oder Keimzelltumoren sollten weder operativ noch radiochirurgisch behandelt werden, es sei denn, dass sie eine klinisch relevante Kompression verursachen. In der Behandlung stehen grundsätzlich Ganzhirnbestrahlung und chemotherapeutische Verfahren im Vordergrund.
In einer retrospektiven Analyse von Bindal et al. (1993) zeigte sich, dass auch Patienten mit multiplen Metastasen erfolgreich operativ behandelt werden können und Überlebensraten erreichen können, die denen von Patienten mit singulären Metastasen vergleichbar sind. Allerdings handelte es sich hier um ein nicht repräsentatives, hoch selektioniertes Patientengut. Ein invasiveres Vorgehen sollte bis auf seltene Fälle, mit sehr gutem klinischen Zustand und günstig gelegenen Läsionen nicht empfohlen werden.
Ganzhirnbestrahlung (GSB)
Die Ganzhirnbestrahlung ist die Methode der Wahl bei sehr vielen zerebralen Metastasen. Die Rolle der GSB als Begleittherapie nach oder vor der Radiochirurgie ist kontrovers diskutiert in der Literatur. Die Möglichkeit eine Progression der Hirnmetastasierung durch regelmäßige MRT Untersuchungen (alle 3-4 Monate in den ersten 3 Jahren) rechtzeitig zu entdecken und die Gesamtprognose des Patienten sollten im Entscheidungsprozess eine wichtige Rolle spielen.
Nach GSB tritt eine komplette Alopezie auf, die aber in der Regel reversibel ist. In isolierten Fällen sind Spätfolgen im Sinne von kognitiven Störungen bis zur Demenz beschrieben (DeAngelis et al. 1989). Morphologische Veränderungen wie Hirnatrophie oder Leukoencephalopathie sind auf den MRT-Aufnahmen häufig nach der Therapie zu beobachten, bleiben aber in der Regel ohne klinisches Korrelat.
Chemotherapie
Die Chemotherapie hat bisher bei der Behandlung von Patienten mit Hirnmetastasen noch keinen klar definierten Stellenwert im Behandlungskonzept. Die Annahme, dass die Blut-Hirnschranke die Penetration von Chemotherapeutika in die befallenen Areale im ZNS verhindert, war der Grund dafür, beim Vorliegen von Hirnmetastasen bevorzugt die Strahlentherapie einzusetzen und der Chemotherapie selten oder nie den Vorzug zu geben. In einigen klinischen Studien konnte jedoch gezeigt werden, dass die Blut-Hirnschranke nicht der entscheidende Faktor ist, der eine erfolgreiche Chemotherapie von Hirnmetastasen vereitelt. Chemotherapien wurden erfolgreich bei Hirnmetastasen von systemisch nicht vorbehandelten Patienten mit kleinzelligem Bronchialkarzinom (Kristensen et al. 1992), Mammakarzinom (Boogerd et al. 1992) und Keimzelltumoren (Fossa et al. 1999) eingesetzt. Bei Verwendung der sonst üblichen Chemotherapieschemata waren die Tumorrückbildungsraten gleich hoch wie bei ausschließlich extrakranieller Metastasierung und der Strahlentherapie nicht unterlegen. In einer Übersichtsarbeit werden die Ergebnisse von 12 Patientenserien an 116 Patienten mit metastasiertem kleinzelligem Bronchialkarzinom zusammengefasst (Kristensen et al. 1992). Die Ansprechrate der Hirnmetastasen auf eine alleinige Chemotherapie ohne zusätzliche Strahlentherapie lag bei 76 % und bei immerhin 43 %, wenn sie im Falle eines Rezidivs nach Ganzhirnbestrahlung zur Anwendung kam.
Partnerschaften